每日經濟新聞 2019-08-22 21:04:40
藥品管理法修訂草案二次審議稿規定:疫苗、血液制品、麻醉藥品、精神藥品、醫療用毒性藥品、放射性藥品等國家實行特殊管理的藥品不得在網絡上銷售。
每經記者|周程程 每經編輯|陳旭
8月22日,藥品管理法修訂草案提請十三屆全國人大常委會第十二次會議審議。
《每日經濟新聞》記者注意到,人民群眾關心的諸多問題,在此次修訂草案二次審議稿中都作出了明確規定。
例如,修訂草案二次審議稿對假藥劣藥范圍進行重新界定。對于備受關注的網絡售藥方面,修訂草案二次審議稿也明確:網絡銷售藥品應當遵守藥品經營的有關規定,并授權相關部門制定具體管理辦法。
此外在藥品審評審批方面,修訂草案二次審議稿明確對“防治重大傳染病和罕見病等疾病的新藥、兒童用藥品”予以優先審評審批。
藥品關乎人民群眾健康,那么到底應該如何科學界定何為假藥、劣藥?
全國人民代表大會憲法和法律委員會關于《中華人民共和國藥品管理法(修訂草案)》審議結果的報告中介紹,有的常委會組成人員、部門、專家和社會公眾提出,現行法律對假藥劣藥范圍的界定比較寬泛,既有根據藥品質量界定的假藥劣藥,又有未經審批生產的藥品等按假藥劣藥論處的情形,不便于精準懲治,建議主要按照藥品功效重新界定假藥劣藥范圍。
對此,修訂草案二次審議稿明確假藥包括:所含成分與國家藥品標準規定的成分不符的藥品,以非藥品冒充藥品或者以他種藥品冒充此種藥品,變質的藥品,所標明的適應癥或者功能主治超過規定范圍的藥品。
劣藥包括:成分含量不符合國家藥品標準的藥品,被污染的藥品,未標明或者更改有效期、超過有效期、未注明或者更改產品批號的藥品,擅自添加防腐劑和輔料的藥品,其他不符合藥品標準的藥品。
值得注意的是,二次審議稿同時對原“按假藥論處”“按劣藥論處”情形中國務院藥品監督管理部門禁止使用的藥品,必須批準而未經批準生產、進口的藥品,必須檢驗而未經檢驗即銷售的藥品,使用必須批準而未經批準的原料藥生產的藥品,使用未經批準的直接接觸藥品的包裝材料和容器生產的藥品,單獨作出規定,明確禁止生產、進口、銷售這些藥品,并從嚴規定處罰。
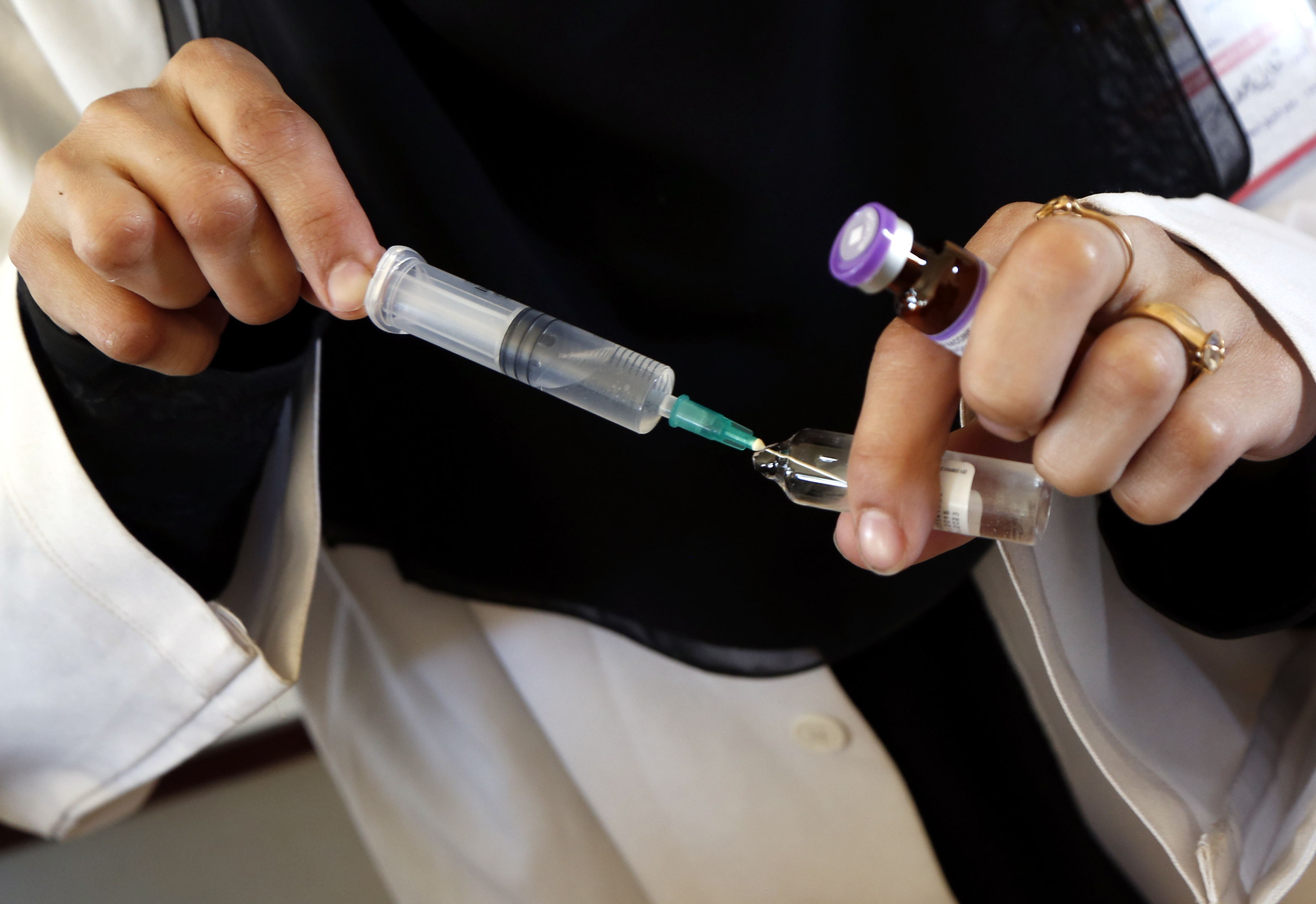
圖片來源:新華社
此前,有的常委會委員、部門、專家和社會公眾建議鼓勵藥品零售連鎖經營,明確藥師職責,加強網絡銷售藥品監管,細化醫療機構臨床急需進口少量藥品的要求。
對此,修訂草案二次審議稿中增加規定國家鼓勵、引導藥品零售連鎖經營,從事藥品零售連鎖經營活動的企業總部,應當建立統一的質量管理制度,對所屬零售企業的經營活動履行管理責任。同時明確藥品經營企業和醫療機構的藥師負責本單位的藥品管理、處方審核和調配、合理用藥指導等工作。明確經批準醫療機構因臨床急需可以進口少量藥品,在指定醫療機構內用于特定醫療目的。
針對網絡售藥方面,修訂草案二次審議稿第六十一條規定,藥品上市許可持有人、藥品經營企業通過網絡銷售藥品,應當遵守本法藥品經營的有關規定。疫苗、血液制品、麻醉藥品、精神藥品、醫療用毒性藥品、放射性藥品等國家實行特殊管理的藥品不得在網絡上銷售。通過網絡銷售藥品的具體管理辦法,由國務院藥品監督管理部門會同國務院衛生健康主管部門等部門制定。
此外,全國人大憲法和法律委員會在報告中指出,有的常委會組成人員和社會公眾提出,應當采取措施保障基本藥物供應,通過對罕見病用藥等藥品給予優先審評審批增加供應。
對此,修訂草案二次審議稿中增加規定國家遴選適當數量的基本藥物品種,加強組織生產和儲備,提高基本藥物的供給能力,滿足疾病防治基本用藥需求。同時,明確對“防治重大傳染病和罕見病等疾病的新藥、兒童用藥品”予以優先審評審批。
封面圖片來源:新華社
如需轉載請與《每日經濟新聞》報社聯系。
未經《每日經濟新聞》報社授權,嚴禁轉載或鏡像,違者必究。
讀者熱線:4008890008
特別提醒:如果我們使用了您的圖片,請作者與本站聯系索取稿酬。如您不希望作品出現在本站,可聯系我們要求撤下您的作品。
歡迎關注每日經濟新聞APP
